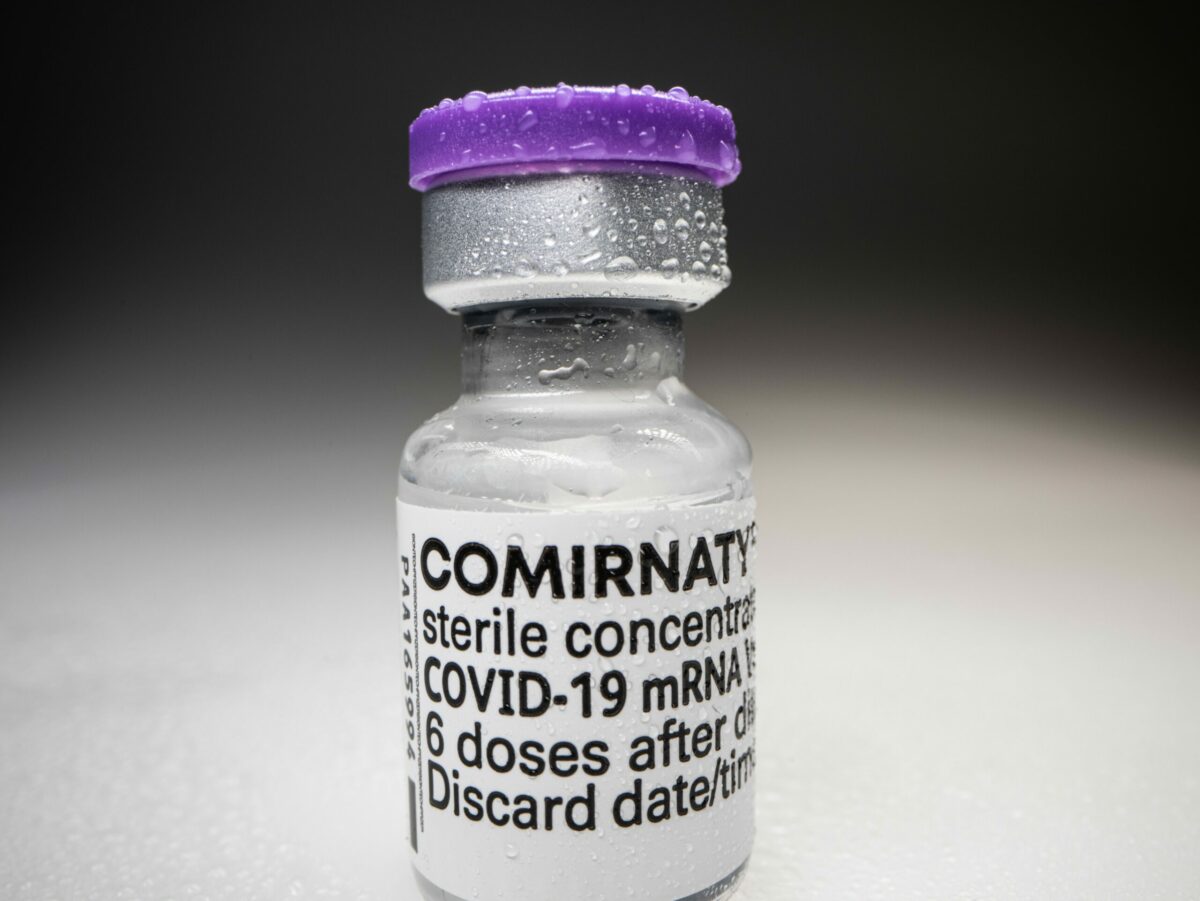
FDA: Vollständige Zulassung für Comirnaty
Die US-Arzneimittelbehörde FDA hat dem Mittel des deutschen Herstellers BioNTech und seines US-Partners Pfizer als erstem Corona-Impfstoff in den USA die vollständige Zulassung erteilt. Sie gelte für Menschen ab 16 Jahren, teilte die FDA am Montag mit und nannte die Entscheidung einen „Meilenstein“ im Kampf gegen die Pandemie. Die Notfallzulassung für Personen ab zwölf Jahren bleibe weiterhin bestehen.
Der Impfstoff ist in den USA seit Dezember mit einer Notfallzulassung im Einsatz, im Mai hatten BioNTech und Pfizer die vollständige Zulassung beantragt. Dafür musste die FDA, die ein beschleunigtes Verfahren nutzte, etwa zehnmal so viele Daten prüfen wie für die Notfallzulassung – darunter viele, die aus dem massenhaften Einsatz des Impfstoffs im Land in den vergangenen Monaten gewonnen wurden.
Die vollständige Zulassung könnte den Erwartungen vieler Expert:innen zufolge weitere Impfpflichten nach sich ziehen – etwa von Stadtverwaltungen, Universitäten oder Gesundheitseinrichtungen, die unter anderem aus rechtlichen Gründen die vollständige Zulassung für einen solchen Schritt abwarten wollten. Zudem erhoffen sich Expert:innen auch davon abgesehen einen Schub für die Impfkampagne, da viele Menschen, die sich bislang nicht haben impfen lassen, in Umfragen das Fehlen einer vollständigen Zulassung als Grund dafür angaben. Dies könnte womöglich aber auch nur als Vorwand angegeben worden sein.
Auch die Impfstoffe von Moderna und Johnson & Johnson werden in den USA bereits seit Monaten basierend auf Notfallzulassungen eingesetzt. Moderna hat Anfang Juni die vollständige Zulassung bei der FDA beantragt, allerdings noch nicht alle Dokumente dafür eingereicht. Johnson & Johnson will einen solchen Antrag noch in diesem Jahr stellen.
Das könnte dich auch interessieren
Mehr aus dieser Kategorie
Sildenafil als „Knochenbooster“?
Sildenafil gehört zu den Mitteln der Wahl zur Behandlung einer erektilen Dysfunktion (ED). Dafür bedarf es einer ärztlichen Verschreibung, denn …
„Cocaine kills brain“: Warnung vor Hirnschäden durch Kokain
Vom Kultgetränk zur Kultdroge: Während Kokain bis ins 20. Jahrhundert meist über „Kokain-Cola“ konsumiert werden konnte, unterliegt die Substanz heutzutage …
Rezeptur 1×1: Mometasonfuroat-Creme
Ob Wirkstoffe, Zubereitung oder Wechselwirkungen – nicht nur bei der Beratung im HV, sondern auch in der Rezeptur ist dein …